-
製剤写真・
組成・性状 - お知らせ
- コード・番号表
- FAQ
- 電子添文
- インタビューフォーム
-
くすりのしおり
(日本語) -
くすりのしおり
(英語) - 適正使用ガイド
- RMP
-
患者向
医薬品ガイド - 製造販売後調査
- 患者指導箋
-
その他の
適正使用資料
製剤写真・組成・性状
組成・性状
| 成分名 | テルミサルタン/ヒドロクロロチアジド |
|---|---|
| 領域名 | 循環器疾患 |
| 成分・含量 | 1錠中 テルミサルタン 80mg ヒドロクロロチアジド 12.5mg |
| 剤形・色調 | 黄橙色の素錠 |
| 外形 |
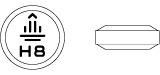
|
| 識別コード | 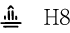 |
| 直径 | 約11mm |
| 厚さ | 約4.1mm |
| 重さ | 約0.48g |
剤形
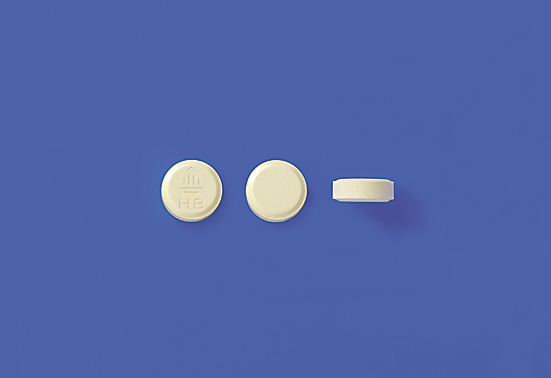
包装形態
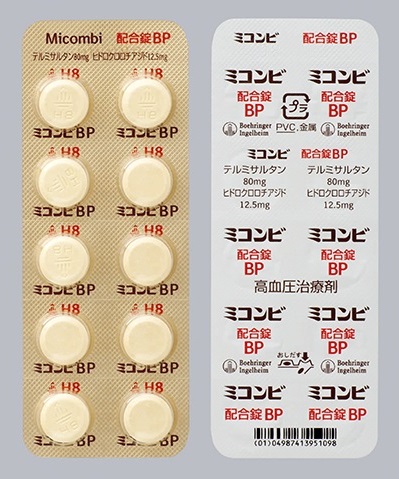
コード・番号表
| 日本標準商品分類番号 | 872149 |
|---|---|
| 承認番号 | 22100AMX00652000 |
| 薬価基準収載 医薬品コード |
2149113F2023 |
| レセプト電算処理コード | 621926701 |
包装:100錠PTP
| JANコード | 4987413670616 |
|---|---|
| HOT7(処方用番号) | 1192674 |
| HOT番号 | 1192674020101 |
| 販売包装単位コード | (01)14987413670613 |
| 調剤包装単位コード | (01)04987413951098 |
よくある質問
-
本剤の電子添文上、胆嚢を摘出した患者への投与に関する注意喚起を行っておりません。
電子添文上の禁忌は、胆嚢の有無ではなく、「胆汁の分泌が極めて悪い患者又は重篤な肝障害のある患者」です。患者さんの個々の状態に応じてご判断をお願い致します。<参考>
本剤の成分であるテルミサルタンは未変化体としてはほとんど尿中に排泄されず、大部分が胆汁を介して、グルクロン酸抱合体として糞中に排泄される。
従って、胆汁の排泄が途絶えているような患者や重篤な肝障害のある患者では本剤が体外に排泄されず蓄積するおそれがある。<引用>
ミコンビ配合錠 電子添文
ミコンビ配合錠 インタビューフォーム Ⅷ.安全性(使用上の注意等)に関する項目 2.禁忌内容とその理由 -
本剤の簡易懸濁法による投与はお勧めできません。
-
本剤の粉砕投与は承認された用法ではないので、お勧めはできません。
-
本剤に割線はありません。
また、半錠での投与は承認された用法ではないため、お勧めはできません。
なお、半錠での安定性に関する検討は行っておりません。 -
本剤の分包後は吸湿して軟化することがあるので、高温・多湿を避けて保存いただくようにお願いします。
<参考>
無包装状態で、25℃/93%R.H.(暗所)の条件にて1ヶ月保存したところ、吸湿し、軟化した。
無包装状態で、25℃/75%R.H.(暗所)の条件での1ヶ月保存においては、分解物が生成したが、規格内であった。
また、無包装状態でキセノンランプ照射下(約25℃)、120万ルクス・hでの保存では、分解物が生成したが、規格内であった。<引用>
ミコンビ配合錠 電子添文
ミコンビ配合錠 インタビューフォーム Ⅳ.製剤に関する項目 6.製剤の各種条件下における安定性