製剤写真・組成・性状
組成・性状
| 成分名 | エンパグリフロジン |
|---|---|
| 領域名 | 循環器疾患、代謝系疾患、慢性腎臓疾患 |
| 成分・含量 | 1錠中エンパグリフロジン10mg |
| 剤形・色調 | 淡黄色のフィルムコート錠 |
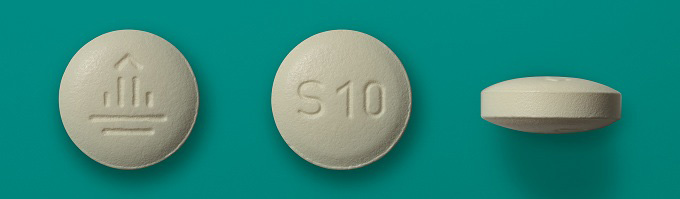
| 外形 |

|
| 識別コード | 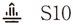 |
| 直径 | 9.1mm |
| 厚さ | 3.65mm |
| 重さ | 257mg |
剤形
包装形態
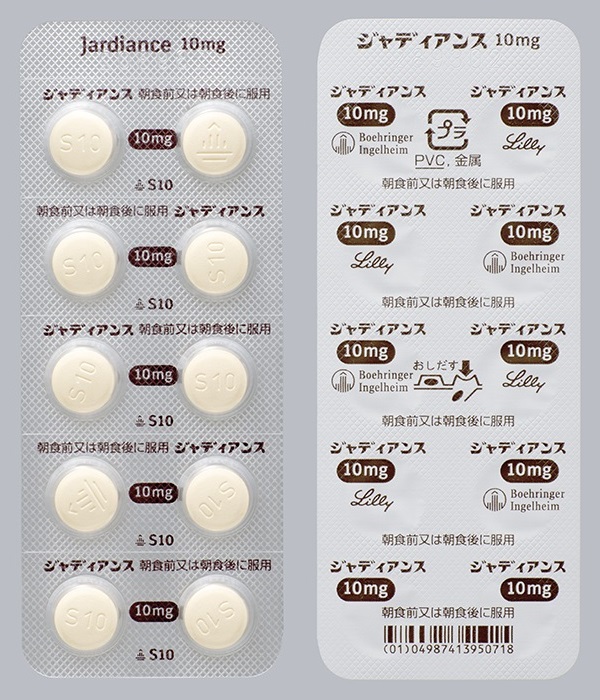
10錠(PTP)包装変更前
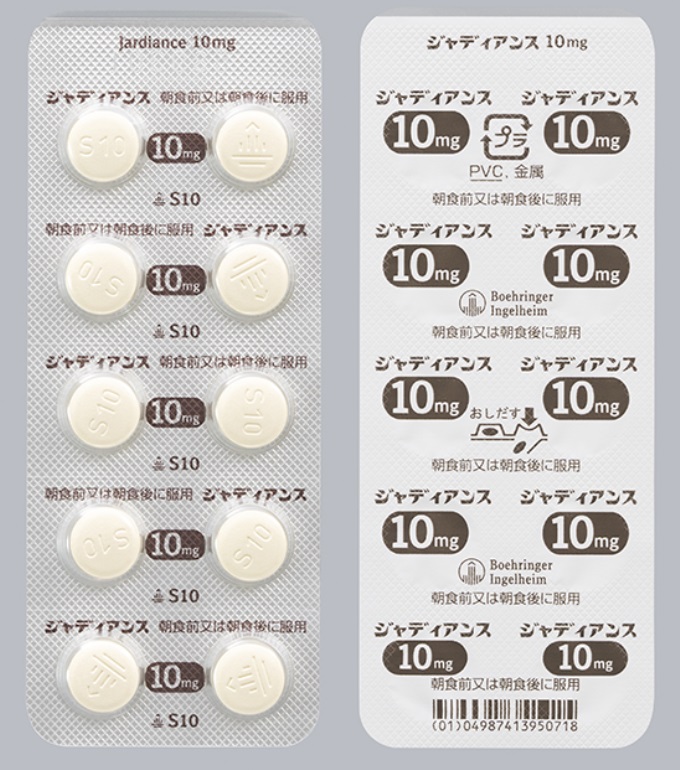
10錠(PTP)包装変更後
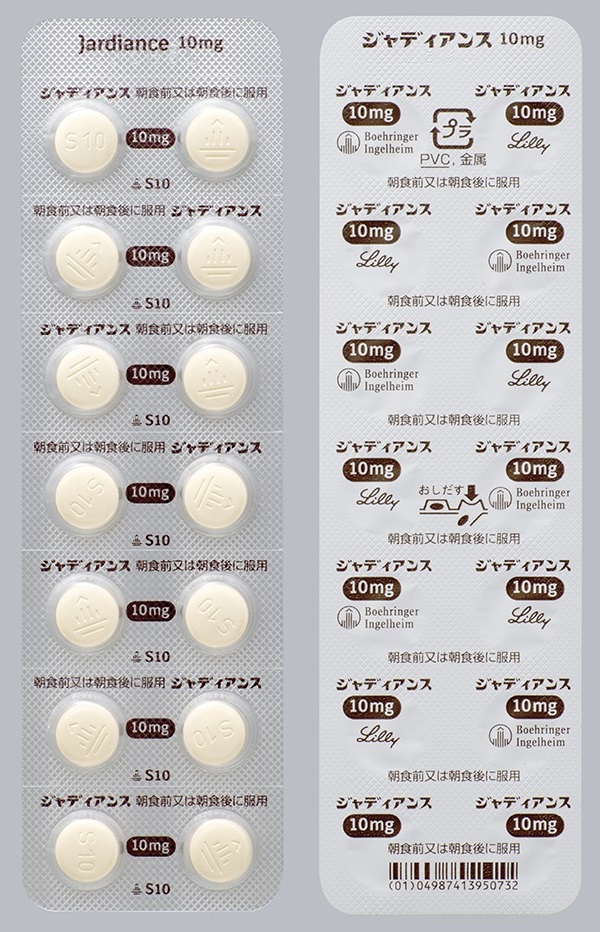
14錠(PTP)包装変更前
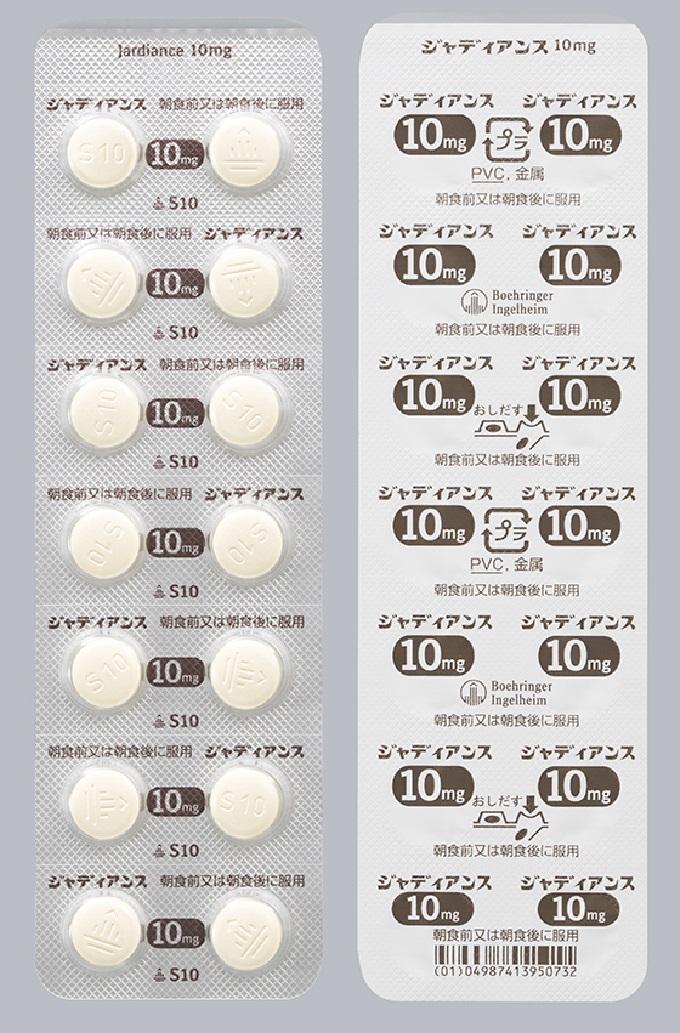
14錠(PTP)包装変更後
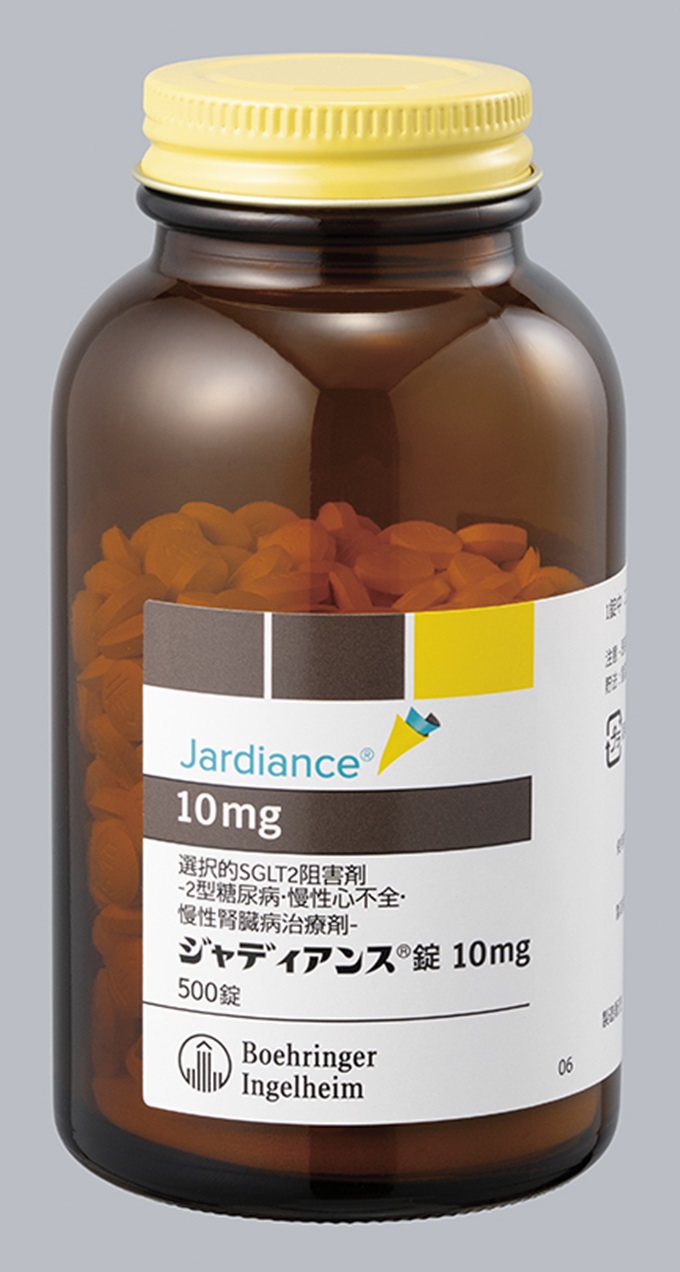
500錠(瓶、バラ)
コード・番号表
| 日本標準商品分類番号 | 873969 |
|---|---|
| 承認番号 | 22600AMX01387000 |
| 薬価基準収載 医薬品コード |
3969023F1023 |
| レセプト電算処理コード | 622401201 |
包装:100錠(10錠×10)PTP
| JANコード | 4987413300612 |
|---|---|
| HOT7(処方用番号) | 1240122 |
| HOT番号 | 1240122010101 |
| 販売包装単位コード | (01)14987413300619 |
| 調剤包装単位コード | (01)04987413950718 |
包装:700錠(14錠×50)PTP
| JANコード | 4987413300643 |
|---|---|
| HOT7(処方用番号) | 1240122 |
| HOT番号 | 1240122010201 |
| 販売包装単位コード | (01)14987413300640 |
| 調剤包装単位コード | (01)04987413950732 |
包装:500錠瓶
| JANコード | 4987413300636 |
|---|---|
| HOT7(処方用番号) | 1240122 |
| HOT番号 | 1240122010301 |
| 販売包装単位コード | (01)14987413300633 |
| 調剤包装単位コード | (01)04987413950725 |
よくある質問
-
<2型糖尿病>
SGLT2阻害薬など他剤からの切り替えを含めて、本剤を開始する場合には10mgからのご使用をお願いいたします。
本剤の10mgで効果不十分な場合には、経過を十分に観察しながら25mgに増量することが可能です。<慢性心不全、慢性腎臓病>
本剤の慢性心不全に対する用法及び用量は10mgのみです。<参考>
●2型糖尿病
通常、成人にはエンパグリフロジンとして10mgを1日1回朝食前又は朝食後に経口投与する。なお、効果不十分な場合には、経過を十分に観察しながら25mg1日1回に増量することができる。
●慢性心不全、慢性腎臓病
通常、成人にはエンパグリフロジンとして10mgを1日1回朝食前又は朝食後に経口投与する。<引用>
ジャディアンス錠 電子添文 -
本剤の簡易懸濁法での投与は承認された用法ではないので、お勧めはできません。
尚、社内試験の結果は55℃の水20 mLに対して5分で崩壊しました。
また,調製した懸濁液はチューブを通過しました。<参考>
試験方法
シリンジに錠剤1 個と約55℃の水20 mL を入れ,錠剤の崩壊性を調査した。
別に粉砕した錠剤を用いて調製した懸濁液がチューブを通過できるかどうかを評価した。
調製直後及び10 分間放置後の懸濁液の含量及びpH を測定した。試験結果
項目 結果 ジャディアンス錠10㎎ ジャディアンス錠25㎎ 崩壊 5分で崩壊した 5分で崩壊した チューブ通過 8Frサイズのチューブを通過した 8Frサイズのチューブを通過した pH 10分放置後7.39(懸濁直後7.41) 10分放置後7.39(懸濁直後7.41) 含量 10分放置後98.6%(懸濁直後97.9%) 10分放置後97.6%(懸濁直後99.0%) <引用>
1.ジャディアンス錠 インタビューフォーム ⅩⅢ.備 考 1.調剤・服薬支援に際して臨床判断を行うにあたっての参考情報 -
本剤の粉砕投与は承認された用法ではないので、お勧めはできません。
<参考>
・温度と相対湿度(R.H.)をそれぞれ25℃/60%,25℃/75%,30℃/75% の条件下(暗所)に6ヵ月間保存したとき,わずかな吸湿(乾燥減量の増加)が認められたものの,その他の試験項目では変化がなく,6 ヵ月間安定でした。
・40℃/75%の条件下(暗所)に保存したとき,わずかな吸湿(乾燥減量の増加)が認められ,10 mg 錠粉砕品では分解生成物(規格内)が認められたが,その他の試験項目では変化がなく,6 ヵ月間安定でした。
・30℃/92%の条件下(暗所)に保存したとき,1 週間で吸湿(乾燥減量の増加)と含量の低下(規格外)が認められました。
・光照射下(120万 lx・h,200 W・h/m2 以上)では,10 mg 錠粉砕品で分解生成物(規格内)が認められたが,その他の試験項目では変化がなく,安定でした。(引用1)<引用>
1.ジャディアンス錠 インタビューフォーム ⅩⅢ.備 考 1.調剤・服薬支援に際して臨床判断を行うにあたっての参考情報 -
本剤に割線はありません。
また、半錠での投与は承認された用法ではないため、お勧めはできません。
なお、半錠での安定性に関する検討は行っておりません。 -
本剤の一包化につきましては、次のデータを参考にご判断お願い致します。
<参考>
25℃/60%RH、30℃/75%RH、40℃/75%RHにおいて褐色ガラス瓶を開栓して6カ月間保存したところ、乾燥減量及び硬度の変化、40℃/75%RHにて分解物の増加が認められましたが、いずれも規格内でした。<引用>
ジャディアンス錠 インタビューフォーム Ⅳ.製剤に関する項目 6.製剤の各種条件下における安定性